Requirements Management Use Case
In der Medizinprodukteentwicklung ist die Aufrechterhaltung klarer Rückverfolgbarkeit von ersten Anforderungen durch Design und Verifikation entscheidend für die regulatorische Compliance. Der Requirements Management Use Case hilft dir, Compliance mit ISO 13485 und FDA QSR Standards aufrechtzuerhalten, indem er einen strukturierten Ansatz für Requirements Management bietet.
Wie Requirements Management funktioniert
Der Requirements Engineering Use Case bietet einen systematischen Ansatz zum Erfassen, Verwalten und Verifizieren von Anforderungen für dein Medizinprodukt. Er stellt Compliance mit regulatorischen Standards sicher, während gleichzeitig klare Rückverfolgbarkeit von Design Inputs bis zur Validierung aufrechterhalten wird, was einen strukturierten Entwicklungsprozess unterstützt.
KU/KTs

Der Requirements Engineering Use Case in CertHub umfasst folgende Schlüsselkomponenten:
- Requirements – Definieren, was erreicht werden muss, oft abgeleitet von Risk Control Measures.
- Design Input – Spezifikationen und Einschränkungen, die von Anforderungen abgeleitet werden, um die Entwicklung zu leiten.
- Design Output – Das Ergebnis des Designprozesses, generiert aus Design Inputs.
- Verification – Stellt sicher, dass Anforderungen und Design Outputs festgelegte Kriterien erfüllen.
- Risk Control Measures – Maßnahmen oder Prozesse, die implementiert werden, um Risiken zu reduzieren, oft Basis für Anforderungen.
- Validation – Bestätigt, dass das finale System oder Produkt Benutzerbedürfnisse und Zweckbestimmung erfüllt.
Beziehungen in der Requirements Analysis definieren
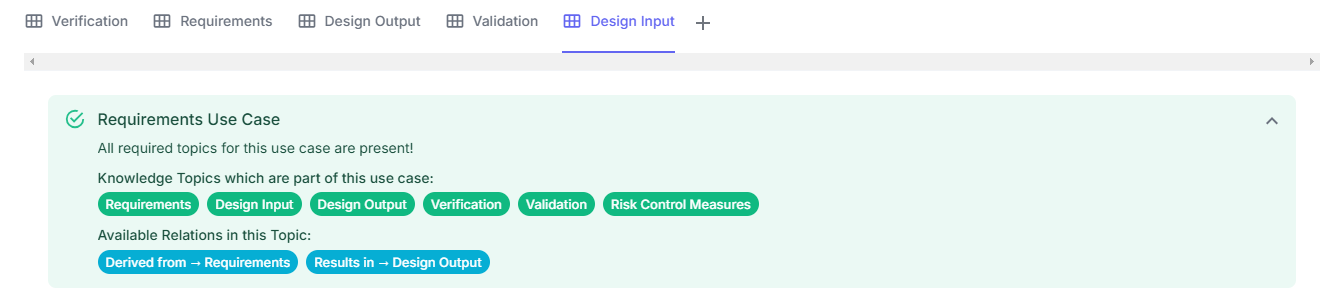
Jedes Knowledge Topic (KT) kann verschiedene Beziehungen haben, die innerhalb der Use Case Konfiguration definiert sind.
| Source Knowledge Topic | Relation Name | Target Knowledge Topic | Allow Multiple | Beschreibung |
|---|---|---|---|---|
| Requirements | Derived from | Risk Control Measures | No | Wähle die Risk Control Measure, die zu dieser Anforderung geführt hat. |
| Implements | Risk Control Measures | Yes | Wähle die Risk Control Measures, die diese Anforderung implementiert. | |
| Derived | Design Input | Yes | Wähle Design Inputs, die von dieser Anforderung abgeleitet wurden. | |
| Verification Tests | Verification | Yes | Wähle Verifikationsaktivitäten, die mit dieser Anforderung verknüpft sind. | |
| Validation Activities | Validation | Yes | Wähle Validierungsaktivitäten, die mit dieser Anforderung verknüpft sind. | |
| Design Input | Derived from | Requirements | No | Wähle die Anforderung, die zu diesem Design Input geführt hat. |
| Results in | Design Output | Yes | Wähle die Design Outputs, die von diesem Input abgeleitet wurden. | |
| Design Output | Generated from | Design Input | No | Wähle den Design Input, der zu diesem Output führt. |
| Verified By | Verification | Yes | Wähle Verifikationsaktivitäten, die Compliance sicherstellen. | |
| Verification | Verifies | Requirements | No | Wähle die Anforderung, die von dieser Aktivität verifiziert wird. |
| Verifies | Design Output | Yes | Wähle Design Outputs, die von dieser Aktivität verifiziert werden. | |
| Risk Control Measures | Implemented By | Requirements | Yes | Wähle Anforderungen, die diese Kontrollmaßnahme implementieren. |
| Verified By | Verification | Yes | Wähle Verifikationsaktivitäten, die die Wirksamkeit der Kontrollmaßnahme sicherstellen. | |
| Validated By | Validation | Yes | Wähle Validierungsaktivitäten, die die Eignung der Kontrollmaßnahme bestätigen. | |
| Validation | Validates | Requirements | No | Wähle die Anforderung, die von dieser Aktivität validiert wird. |
Konkretes Beispiel
Eine spezifisch identifizierte Anforderung wird so gespeichert:
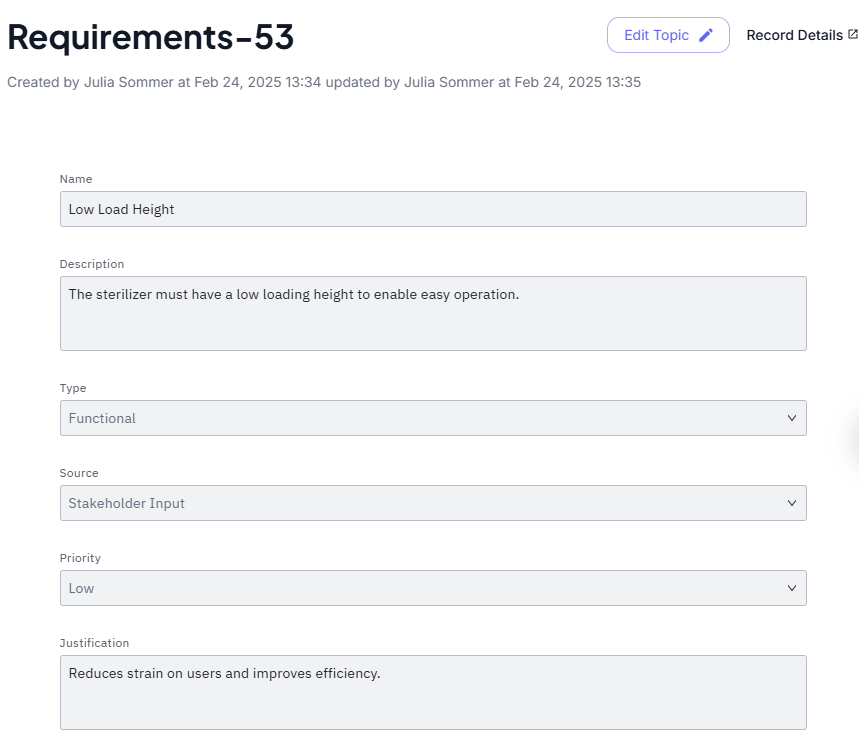
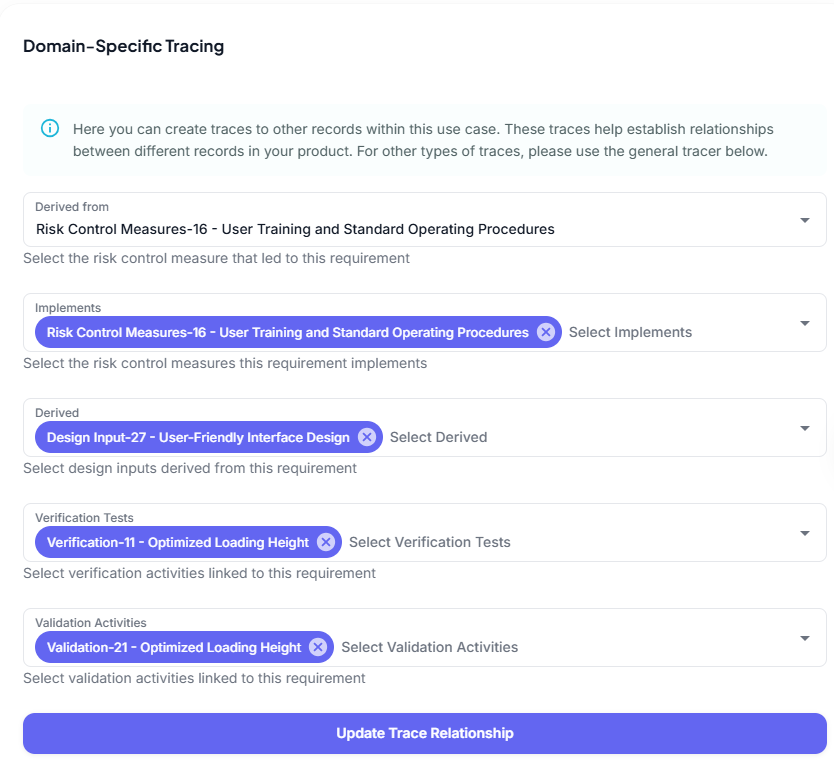
Das ist zum Beispiel eine konkrete Instanz, die eine Beziehung zu einer spezifischen Risk Control Measure, Design Input, Verification und Validation Instanz haben kann.
Templates & Forms
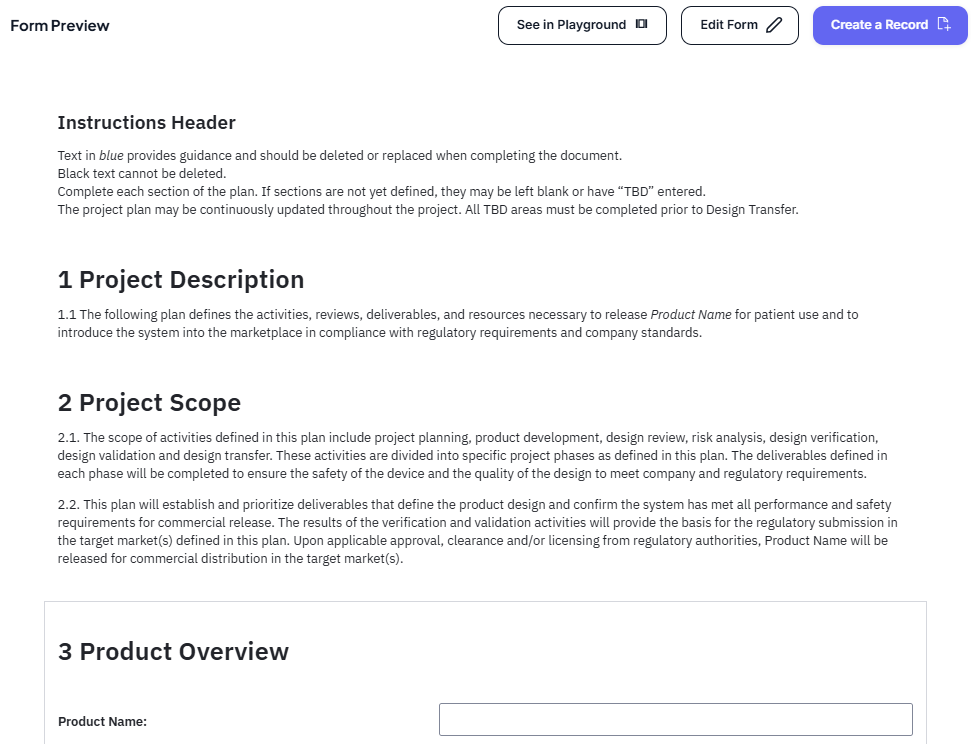
Der Requirements Engineering Use Case umfasst essentielle Templates, um den Entwicklungsprozess effektiv zu strukturieren und zu dokumentieren:
- Requirements List – Erfasst und verfolgt alle Geräteanforderungen und stellt klare Rückverfolgbarkeit sicher.
- Device Design Plan – Skizziert den Design- und Entwicklungsansatz, einschließlich wichtiger Meilensteine und Verantwortlichkeiten.
Diese Templates stellen einen gut organisierten und konformen Requirements Engineering Prozess sicher.
SOPs
Requirements Engineering in CertHub folgt einem strukturierten Prozess:
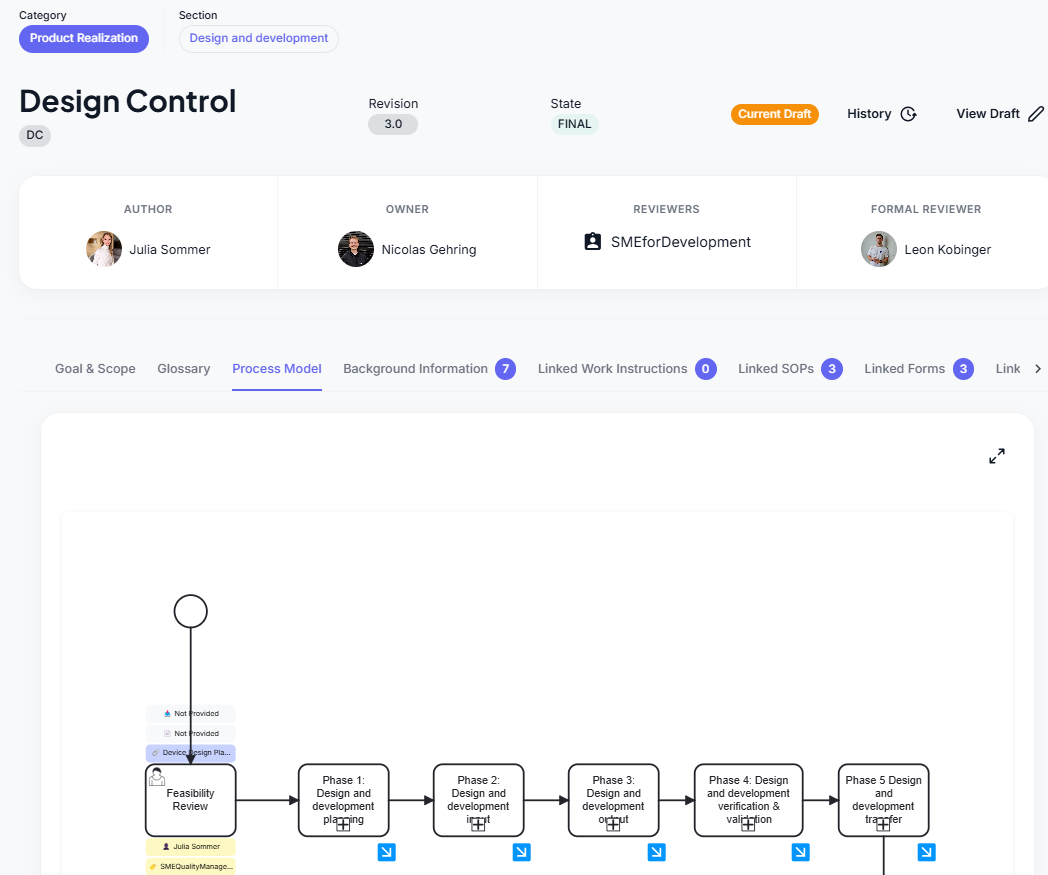
- 🔍 Device Control Process – Definiert, wie Anforderungen während des gesamten Gerätelebenszyklus verwaltet werden, um Compliance und Sicherheit sicherzustellen.
Regulatory Compliance
Der Requirements Management Use Case hilft, wichtige regulatorische Anforderungen zu erfüllen:
- ✅ ISO 13485:7.3 Design and Development
- ✅ FDA 21 CFR 820.30 Design Controls
- ✅ EU MDR Article 10 General Obligations
Durch das Befolgen des strukturierten Ansatzes, den dieser Use Case bietet, kannst du vollständige Requirements-Rückverfolgbarkeit während regulatorischer Audits demonstrieren.
Integration mit anderen Use Cases
Der Risk Management Use Case verbindet sich mit dem Requirements Engineering Use Case durch Risk Control Measures.
Diese Verbindung wird hergestellt, indem das Risk Control Measure Knowledge Topic (KT) in beiden Use Cases enthalten ist.
Durch die Wiederverwendung gemeinsamer KTs macht CertHub die Integration verschiedener Use Cases nahtlos und effizient, was eine reibungslose Rückverfolgbarkeit über Prozesse hinweg sicherstellt.
Schau dir den Risk Management Use Case für weitere Informationen an, wie die Risk Control Measure verwendet wird.